يود
| |||||||||||||||||||||||||||||||
| المظهر | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
رمادي لمّاع في الحالة الصلبة، بنفسجي في الحالة الغازية
| |||||||||||||||||||||||||||||||
| الخواص العامة | |||||||||||||||||||||||||||||||
| الاسم، العدد، الرمز | يود، 53، I | ||||||||||||||||||||||||||||||
| تصنيف العنصر | هالوجين | ||||||||||||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 17، 5، p | ||||||||||||||||||||||||||||||
| الكتلة الذرية | 126.90447 غ·مول−1 | ||||||||||||||||||||||||||||||
| توزيع إلكتروني | Kr]؛ 4d10 5s2 5p5] | ||||||||||||||||||||||||||||||
| توزيع الإلكترونات لكل غلاف تكافؤ | 2, 8, 18, 18, 7 (صورة) | ||||||||||||||||||||||||||||||
| الخواص الفيزيائية | |||||||||||||||||||||||||||||||
| الطور | صلب | ||||||||||||||||||||||||||||||
| الكثافة (عند درجة حرارة الغرفة) | 4.933 غ·سم−3 | ||||||||||||||||||||||||||||||
| نقطة الانصهار | 386.85 ك، 113.7 °س، 236.66 °ف | ||||||||||||||||||||||||||||||
| نقطة الغليان | 457.4 ك، 184.3 °س، 363.7 °ف | ||||||||||||||||||||||||||||||
| نقطة ثلاثية | 386.65 كلفن (113°س)، 12.1 كيلوباسكال |
||||||||||||||||||||||||||||||
| النقطة الحرجة | 819 ك، 11.7 ميغاباسكال | ||||||||||||||||||||||||||||||
| حرارة الانصهار | 15.52 (I2) كيلوجول·مول−1 | ||||||||||||||||||||||||||||||
| حرارة التبخر | 41.57 (I2) كيلوجول·مول−1 | ||||||||||||||||||||||||||||||
| السعة الحرارية (عند 25 °س) | 54.44 (I2) جول·مول−1·كلفن−1 | ||||||||||||||||||||||||||||||
| ضغط البخار | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| الخواص الذرية | |||||||||||||||||||||||||||||||
| أرقام الأكسدة |
7, 5, 3, 1, -1 (أكاسيده حمضية قوية) |
||||||||||||||||||||||||||||||
| الكهرسلبية | 2.66 (مقياس باولنغ) | ||||||||||||||||||||||||||||||
| طاقات التأين | الأول: 1008.4 كيلوجول·مول−1 | ||||||||||||||||||||||||||||||
| الثاني: 1845.9 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||
| الثالث: 3180 كيلوجول·مول−1 | |||||||||||||||||||||||||||||||
| نصف قطر ذري | 140 بيكومتر | ||||||||||||||||||||||||||||||
| نصف قطر تساهمي | 3±139 بيكومتر | ||||||||||||||||||||||||||||||
| نصف قطر فان دير فالس | 198 بيكومتر | ||||||||||||||||||||||||||||||
| خواص أخرى | |||||||||||||||||||||||||||||||
| البنية البلورية | نظام بلوري معيني قائم | ||||||||||||||||||||||||||||||
| المغناطيسية | مغناطيسية معاكسة | ||||||||||||||||||||||||||||||
| مقاومة كهربائية | 1.3×107أوم·متر (0 °س) | ||||||||||||||||||||||||||||||
| الناقلية الحرارية | 0.449 واط·متر−1·كلفن−1 (300 كلفن) | ||||||||||||||||||||||||||||||
| معامل الحجم | 7.7 غيغاباسكال | ||||||||||||||||||||||||||||||
| رقم CAS | 7553-56-2 | ||||||||||||||||||||||||||||||
| النظائر الأكثر ثباتاً | |||||||||||||||||||||||||||||||
| المقالة الرئيسية: نظائر اليود | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
اليود هو عنصر كيميائي له الرمز I والعدد الذري 53 في الجدول الدوري. ينتمي إلى فصيلة الهالوجينات.
غازه يحول ورقة النشا إلى اللون الأزرق كما هو معروف وإذا تفاعل مع نترات الفضة يكون راسب أصفر من يوديد الفضة وكذلك الأمر إذا تفاعل أحد أملاحه مع أسيتات الرصاص وإذا تفاعل مع كبريتات النحاس كون لنا راسب بني ومع كلوريد الزئبق كون لنا راسب أحمر وهو غازى أصلاً في الحالة العادية لكنه يتم حفظه في الصورة الصلبة حيث يتميز بخاصية التسامى «أي تحول العنصر من الحالة الصلبة إلى الحالة الغازية دون المرور بالحالة السائلة». عنصر اليود يوجد في العديد من الاطعمه مثل الاسماك
المنتجان المهيمنان لليود اليوم هما تشيلي واليابان. يستخدم اليود ومركباته بشكل أساسي في التغذية. نظرًا لارتفاع عددها الذري وسهولة ارتباطها بالمركبات العضوية، فقد وجدت أيضًا ميزة كمواد تباين إشعاعي غير سامة. بسبب خصوصية امتصاصه من قبل جسم الإنسان، يمكن أيضًا استخدام النظائر المشعة لليود لعلاج سرطان الغدة الدرقية. يستخدم اليود أيضًا كعامل مساعد في الإنتاج الصناعي لحمض الخليك وبعض البوليمرات
وهو مدرج في قائمة منظمة الصحة العالمية للأدوية الأساسية.
تاريخ
في عام 1811، اكتشف الكيميائي الفرنسي برنارد كورتوا اليود، الذي ولد لمصنع الملح الصخري (مكون أساسي من البارود). في وقت الحروب النابليونية، كان هناك طلب كبير على الملح الصخري في فرنسا. الملح الصخري المستخرج من الفرنسية سرير ملح البارود المطلوبة كربونات الصوديوم، والتي يمكن أن تكون معزولة من الأعشاب البحرية التي تم جمعها على سواحل نورماندي وبريتاني. لعزل كربونات الصوديوم تم حرق الطحالب البحرية وغسل الرماد بالماء. تم إتلاف النفايات المتبقية عن طريق إضافة حامض الكبريتيك. أضاف كورتوا مرة حمض الكبريتيك المفرط وارتفعت سحابة من البخار الأرجواني. وأشار إلى أن البخار يتبلور على الأسطح الباردة مكونًا بلورات داكنة. شك كورتوا في أن هذه المادة كانت عنصرًا جديدًا لكنها كانت تفتقر إلى التمويل لمتابعة ذلك.
أعطى كورتوا عينات لأصدقائه، تشارلز برنارد ديسورمس (1777-1838) ونيكولاس كليمان (1779-1841)، لمواصلة البحث. كما أعطى بعضًا من هذه المادة للكيميائي جوزيف لويس جاي لوساك (1778-1850) والفيزيائي أندريه ماري أمبير (1775-1836). في 29 نوفمبر 1813، أعلن ديسورمز وكليمان اكتشاف كورتوا للجمهور. وصفوا المادة لاجتماع المعهد الإمبراطوري في فرنسا. في 6 ديسمبر، أعلن جاي لوساك أن المادة الجديدة كانت إما عنصرًا أو مركبًا من الأكسجين. اقترح جاي لوساك اسم "iode" من اليونانية القديمة ἰοειδής (ioeidēs، «البنفسجي»)، بسبب لون بخار اليود. أعطى أمبير بعضًا من عيّنته للكيميائي الإنجليزي همفري ديفي (1778-1829)، الذي أجرى تجارب على المادة ولاحظ تشابهها مع الكلور. أرسل ديفي رسالة مؤرخة في 10 ديسمبر إلى الجمعية الملكية في لندن تفيد بأنه قد حدد عنصرًا جديدًا. اندلعت الجدل بين ديفي وجاي لوساك حول من حدد اليود أولاً، لكن كلا العالمين اعترف بأن كورتوا هو أول من عزل العنصر.
اكتشف الباحث الطبي الفرنسي كازيمير جوزيف دافين (1812-1882) في عام 1873 مفعول اليود المطهر.كان أنطونيو غروسيش (1849-1926)، جراحًا من مواليد إستريا، من بين أول من استخدم تعقيم مجال الجراحة. في عام 1908، قدم صبغة اليود كوسيلة لتعقيم جلد الإنسان بسرعة في مجال الجراحة.
في الجداول الدورية المبكرة، غالبًا ما كان يتم إعطاء اليود الرمز J، بالنسبة اسمه باللغة الألمانية.
الخصائص
اليود هو الهالوجين الرابع، كونه عضو في المجموعة 17 في الجدول الدوري، تحت الفلور والكلور والبروم؛ إنه أثقل عضو مستقر في مجموعته. (لم يتم دراسة الهالوجين الخامس والسادس، الأستاتين المشع والتينيسين، جيدًا بسبب تكلفتهما وعدم إمكانية الوصول إليهما بكميات كبيرة، ولكن يبدو أنهما يظهران خصائص مختلفة غير عادية للمجموعة بسبب التأثيرات النسبية). يحتوي اليود على تكوين إلكترون لـ [Kr] 4d 10 5s 2 5p 5، مع الإلكترونات السبعة في الغلاف الخامس والأبعد من الغلاف الخارجي هي إلكترونات التكافؤ. مثل الهالوجينات الأخرى، فهو إلكترون واحد ينقصه ثماني بتات كاملة، وبالتالي فهو عامل مؤكسد، يتفاعل مع العديد من العناصر من أجل إكمال غلافه الخارجي، على الرغم من أنه تمشيا مع الاتجاهات الدورية، فهو أضعف عامل مؤكسد بين الهالوجينات المستقرة: لديه أدنى قدر من السالبية الكهربية فيما بينها، فقط 2.66 على مقياس بولينج (قارن الفلور والكلور والبروم عند 3.98 و3.16 و2.96 على التوالي؛ يواصل الأستاتين الاتجاه بقدرة كهربية 2.2). ومن ثم فإن عنصر اليود يشكل جزيئات ثنائية الذرة مع الصيغة الكيميائية I 2، حيث تشترك ذرتان من اليود في زوج من الإلكترونات من أجل تحقيق كل منهما ثماني بتات مستقرة؛ في درجات حرارة عالية، هذه الجزيئات ثنائية الذرة تفصل بشكل عكسي زوج من ذرات اليود. وبالمثل، فإن أنيون اليوديد، I -، هو أقوى عامل مختزل بين الهالوجينات المستقرة، لأنه الأكثر تأكسدًا بسهولة إلى ثنائي الذرة I 2. (يذهب أستاتين إلى أبعد من ذلك، كونه غير مستقر بالفعل مثل At - ويتأكسد بسهولة إلى عند 0 أو عند +، على الرغم من عدم تسوية وجود At 2.)
يتحول لون الهالوجينات إلى اللون الغامق مع نزول المجموعة: الفلور أصفر شاحب للغاية، والكلور أصفر مخضر، والبروم بني محمر، واليود بنفسجي.
عنصر اليود قابل للذوبان بشكل طفيف في الماء، ويذوب جرام واحد في 3450 مل عند 20 درجة مئوية و1280 مل عند 50 درجة مئوية؛ يوديد البوتاسيوم قد تضاف إلى زيادة القابلية للذوبان عبر تشكيل ثلاثي اليوديد الأيونات، بين بوليوديد الآخرين. توفر المذيبات غير القطبية مثل الهكسان ورابع كلوريد الكربون قابلية ذوبان أعلى. المحاليل القطبية، مثل المحاليل المائية، بنية اللون، مما يعكس دور هذه المذيبات كقواعد لويس؛ من ناحية أخرى، المحاليل غير القطبية هي البنفسجي، لون بخار اليود.تتشكل معقدات نقل الشحنة عندما يذوب اليود في مذيبات قطبية، وبالتالي يتغير اللون. يكون اليود بنفسجي عندما يذوب في رابع كلوريد الكربون والهيدروكربونات المشبعة ولكنه بني غامق في الكحولات والأمينات، المذيبات التي تشكل مقاربات نقل الشحنة.
نقاط انصهار وغليان اليود هي الأعلى بين الهالوجينات، بما يتوافق مع الاتجاه المتزايد أسفل المجموعة، نظرًا لأن اليود يحتوي على أكبر سحابة إلكترونية من بينها والتي يسهل استقطابها، مما يؤدي إلى أن جزيئاته تتمتع بأقوى تفاعلات فان دير فال بين الهالوجينات. وبالمثل، فإن اليود هو أقل الهالوجينات تطايرًا، على الرغم من أن المادة الصلبة لا تزال تُطلق بخارًا أرجوانيًا. بسبب هذه الخاصية، يتم استخدام اليود بشكل شائع لإثبات التسامي مباشرة من المادة الصلبة إلى الغاز، مما يؤدي إلى سوء فهم أنه لا يذوب في الضغط الجوي. نظرًا لأنه يحتوي على أكبر نصف قطر ذري بين الهالوجينات، فإن اليود لديه أقل طاقة تأين أولية، وأقل تقارب للإلكترون، وأدنى كهرسلبية وأقل تفاعل للهالوجينات.
الرابطة بين الهالوجين في الديود هي الأضعف بين جميع الهالوجينات. على هذا النحو، يتم فصل 1٪ من عينة اليود الغازي عند الضغط الجوي إلى ذرات اليود عند 575 درجة مئوية. درجات حرارة أكبر من 750 درجة مئوية مطلوبة لفصل الفلور والكلور والبروم بدرجة مماثلة. معظم روابط اليود أضعف من الروابط المماثلة للهالوجينات الأخف. يتكون اليود الغازي من I 2 جزيئات بطول I-I طول الرابطة 266.6pm . تعتبر رابطة I-I واحدة من أطول الروابط الفردية المعروفة. بل إنها أطول (271.5 pm) في اليود البلوري الصلب لتقويم العظام، والذي له نفس التركيب البلوري مثل الكلور والبروم. (يحتفظ بالسجل زينون جار اليود: طول الرابطة Xe-Xe هو308.71 pm.) هذا النحو، داخل جزيء اليود، تحدث تفاعلات إلكترونية مهمة مع الجارين التاليين الأقرب لكل ذرة، وتؤدي هذه التفاعلات، في كتلة اليود، إلى مظهر لامع وخصائص شبه موصلة. اليود عبارة عن شبه موصل ثنائي الأبعاد بفجوة نطاق تبلغ 1.3 فولت (125 kJ / mol): هو شبه موصل في مستوى طبقاته البلورية وعازل في الاتجاه العمودي.
النظائر
من بين سبعة وثلاثين نظيرًا معروفًا لليود، يوجد واحد فقط في الطبيعة، وهو اليود -127. أما الأنواع الأخرى فهي مشعة ولديها أنصاف عمر أقصر من أن تكون بدائية. على هذا النحو، فإن اليود أحادي النظير وأحادي النواة، ووزنه الذري معروف بدقة كبيرة، لأنه ثابت في الطبيعة.
أطول نظائر اليود المشعة عمرا هو اليود 129، الذي يبلغ نصف عمر نظائره 15.7 مليون سنة، تتحلل عن طريق اضمحلال بيتا إلى زينون مستقر -129. تم تشكيل بعض اليود 129 مع اليود 127 قبل تكوين النظام الشمسي، لكنه تلاشى تمامًا الآن، مما جعله نويدات مشعة منقرضة ومع ذلك لا يزال مفيدًا في تحديد تاريخ النظام الشمسي المبكر أو قديم جدًا. يمكن تحديد وجودها السابق من خلال زيادة ابنتها زينون 129. لا تزال آثار اليود -129 موجودة حتى يومنا هذا، حيث إنه أيضًا نويدات كونية، تكونت من تشظي الأشعة الكونية للزينون الجوي: تشكل هذه الآثار 10 −14 إلى 10 −10 من كل اليود الأرضي. يحدث أيضًا من التجارب النووية في الهواء الطلق، وهو ليس خطيرًا بسبب نصف عمره الطويل بشكل لا يصدق، وهو الأطول بين جميع نواتج الانشطار. في ذروة الاختبارات النووية الحرارية في الستينيات والسبعينيات من القرن الماضي، كان اليود 129 لا يزال يشكل حوالي 10-7 من اليود الأرضي. غالبًا ما تستخدم حالات الإثارة لليود 127 واليود 129 في التحليل الطيفي لموسباور.
والنظائر المشعة الأخرى من اليود لها فترات نصف عمر أقصر بكثير، لا تزيد عن أيام. بعضها له تطبيقات طبية تشمل الغدة الدرقية، حيث يتم تخزين اليود الذي يدخل الجسم وتركيزه. يبلغ عمر النصف لليود 123 ثلاثة عشر ساعة ويتحلل عن طريق التقاط الإلكترون لتيلوريوم 123، مما ينبعث منه إشعاع غاما؛ يتم استخدامه في تصوير الطب النووي، بما في ذلك التصوير المقطعي المحوسب بإصدار فوتون واحد (SPECT) والتصوير المقطعي المحوسب بالأشعة السينية.يبلغ عمر النصف لليود 125 تسعة وخمسين يومًا، ويتحلل عن طريق التقاط الإلكترون إلى التيلوريوم -125 وينبعث منه إشعاع غاما منخفض الطاقة؛ ثاني أطول النظائر المشعة لليود عمرا، يستخدم في المقايسات البيولوجية وتصوير الطب النووي والعلاج الإشعاعي مثل المعالجة الكثبية لعلاج عدد من الحالات، بما في ذلك سرطان البروستاتا والأورام الميلانينية العنبية وأورام المخ. أخيرًا، اليود 131، بعمر نصف يبلغ ثمانية أيام، يتحلل بيتا إلى حالة مثارة من الزينون 131 المستقر الذي يتحول بعد ذلك إلى الحالة الأرضية عن طريق إصدار إشعاع جاما. إنه منتج انشطاري شائع وبالتالي فهو موجود بمستويات عالية في السقوط الإشعاعي. يمكن بعد ذلك امتصاصه من خلال الطعام الملوث، وسوف يتراكم أيضًا في الغدة الدرقية. عندما تتحلل، قد تتسبب في تلف الغدة الدرقية. الخطر الرئيسي من التعرض لمستويات عالية من اليود 131 هو وقوع فرصة الإشعاعية سرطان الغدة الدرقية في الحياة في وقت لاحق. تشمل المخاطر الأخرى احتمال حدوث أورام غير سرطانية والتهاب الغدة الدرقية.
الوسيلة المعتادة للحماية من الآثار السلبية لليود 131 هي عن طريق تشبع الغدة الدرقية باليود المستقر 127 في شكل أقراص يوديد البوتاسيوم، تؤخذ يوميًا للوقاية المثلى. ومع ذلك، يمكن أيضًا استخدام اليود 131 للأغراض الطبية في العلاج الإشعاعي لهذا السبب بالذات، عندما يكون تدمير الأنسجة مطلوبًا بعد امتصاص الأنسجة لليود. يستخدم اليود 131 أيضًا كمتتبع إشعاعي.
الكيمياء والمركبات
| طاقات رابطة الهالوجين (كيلوجول / مول) | |||||
|---|---|---|---|---|---|
| X | XX | HX | BX3 | AlX3 | CX4 |
| فلور | 159 | 574 | 645 | 582 | 456 |
| كلور | 243 | 428 | 444 | 427 | 327 |
| بروم | 193 | 363 | 368 | 360 | 272 |
| يود | 151 | 294 | 272 | 285 | 239 |
اليود شديد التفاعل، لكنه أقل تفاعلًا من الهالوجينات الأخرى. على سبيل المثال، في حين أن غاز الكلور وهالوجينات أول أكسيد الكربون، أكسيد النيتريك، وثاني أكسيد الكبريت (ل الفوسجين، كلوريد نتروزيل، وكلوريد سلفوريل على التوالي) واليود لن تفعل ذلك. علاوة على ذلك، يؤدي إضافة اليود إلى المعادن إلى حالات أكسدة أقل من المعالجة بالكلور أو المعالجة بالبروم؛ على سبيل المثال، يتفاعل معدن الرنيوم مع الكلور لتكوين سداسي كلوريد الرنيوم، ولكن مع البروم فإنه يشكل فقط خماسي بروميد الرينيوم واليود يمكن أن يحقق فقط رباعي يوديد الرينيوم. على نفس المنوال، نظرًا لأن اليود يحتوي على أقل طاقة تأين بين الهالوجينات وأكثرها سهولة في التأكسد، فإنه يحتوي على كيمياء كاتيونية أكثر أهمية وحالات الأكسدة الأعلى الخاصة به أكثر استقرارًا من تلك الموجودة في البروم والكلور سبيل المثال في سباعي فلوريد اليود.
I2 ينفصل في الضوء بامتصاص عند 578 الطول الموجي نانومتر.
مجمعات نقل الشحنات
يذوب جزيء اليود، I 2 ، في CCl 4 والهيدروكربونات الأليفاتية لإعطاء محلول بنفسجي لامع. في هذه المذيبات يحدث أقصى الفرقة امتصاص في – منطقة نانومتر ويتم تعيينها إلى انتقال π * إلى σ *. عندما I 2 يتفاعل مع قواعد لويس في هذه المذيبات ويعتبر تحولا الأزرق في I 2 ذروة وذروة جديدة – نانومتر) يرجع إلى تكوين المقاربات، والتي يشار إليها باسم مجمعات نقل الشحنة.
يوديد الهيدروجين
أبسط مركب من اليود هو يوديد الهيدروجين. إنه غاز عديم اللون يتفاعل مع الأكسجين ليعطي الماء واليود. على الرغم من أنه مفيد في تفاعلات المعالجة باليود في المختبر، إلا أنه ليس له استخدامات صناعية واسعة النطاق، على عكس هاليدات الهيدروجين الأخرى. تجاريًا، يتم تصنيعه عادةً عن طريق تفاعل اليود مع كبريتيد الهيدروجين أو الهيدرازين
2 I 2 + N 2 H 4 H2 O ⟶ 4 HI + N 2
في درجة حرارة الغرفة، يكون غازًا عديم اللون، مثل كل هاليدات الهيدروجين باستثناء فلوريد الهيدروجين، حيث لا يمكن للهيدروجين تكوين روابط هيدروجينية قوية مع ذرة اليود الكبيرة والكهربائية بشكل معتدل. يذوب عند 51.0- درجة مئوية ويغلي عند 35.1- درجة مئوية. إنه مركب ماص للحرارة يمكن أن يتفكك طاردًا للحرارة في درجة حرارة الغرفة، على الرغم من أن العملية بطيئة جدًا ما لم يكن هناك محفز التفاعل بين الهيدروجين واليود عند درجة حرارة الغرفة لإعطاء يوديد الهيدروجين لا يكتمل. طاقة تفكك الرابطة H - I هي بالمثل أصغر هاليدات الهيدروجين، عند 295 كيلوجول / مول.
يُعرف يوديد الهيدروجين المائي باسم حمض الهيدرويودك، وهو حمض قوي. يوديد الهيدروجين قابل للذوبان بشكل استثنائي في الماء لتر واحد من الماء سيذيب 425 لترًا من يوديد الهيدروجين، والمحلول المشبع يحتوي فقط على أربعة جزيئات ماء لكل جزيء من يوديد الهيدروجين. وعادة ما يحتوي ما يسمى بالحمض المائي «المركز» التجاري على 48-57٪ من الكتلة؛ المحلول يشكل أزيوتروب بنقطة غليان 126.7 درجة مئوية عند 56.7 جرام لكل 100جرام الحل. ومن ثم لا يمكن تركيز حمض الهيدرويودك بعد هذه النقطة عن طريق تبخر الماء.
اليودات الثنائية الأخرى
تشكل جميع العناصر الموجودة في الجدول الدوري تقريبًا اليود الثنائي. الاستثناءات هي بالتأكيد أقلية وتنبع في كل حالة من واحد من ثلاثة أسباب: الخمول الشديد والإحجام عن المشاركة في التفاعلات الكيميائية (الغازات النبيلة)؛ عدم الاستقرار النووي الشديد الذي يعيق التحقيق الكيميائي قبل التحلل والتحول (العديد من أثقل العناصر بعد البزموت)؛ ولها قدرة كهرومغناطيسية أعلى من اليود (الأكسجين والنيتروجين والهالوجينات الثلاثة الأولى)، بحيث لا تكون المركبات الثنائية الناتجة بشكل رسمي من اليود بل بالأحرى أكاسيد أو نيتريدات أو هاليدات اليود. (ومع ذلك، يُطلق على ثلاثي يود النيتروجين اسم يوديد لأنه مشابه لثلاثي هاليدات النيتروجين الأخرى.)
ونظرا لحجم كبير من أنيون يوديد واليود وضعف القدرة المؤكسدة، التأكسد عالية يصعب تحقيقه في اليود الثنائية، والحد الأقصى المعروف يجري في خماسيات من النيوبيوم، التنتالوم وبالبروتكتينيوم. يمكن صنع اليود عن طريق تفاعل عنصر أو أكسيده أو هيدروكسيده أو كربوناته مع حمض الهيدرويودك، ثم يتم تجفيفه بدرجات حرارة مرتفعة بشكل معتدل مقترنة إما بضغط منخفض أو غاز يوديد الهيدروجين اللامائي. تعمل هذه الطرق بشكل أفضل عندما يكون منتج اليوديد مستقرًا للتحلل المائي؛ بخلاف ذلك، تشمل الاحتمالات المعالجة باليود المؤكسد بدرجة حرارة عالية للعنصر باليود أو يوديد الهيدروجين، أو المعالجة باليود بدرجة حرارة عالية لأكسيد فلز أو هاليد آخر باليود، أو هاليد فلز متطاير، أو رباعي يوديد كربون، أو يوديد عضوي. على سبيل المثال، يتفاعل أكسيد الموليبدينوم (IV) مع يوديد الألومنيوم (III) عند 230 درجة مئوية لإعطاء يوديد الموليبدينوم (II). فيما يلي مثال يتضمن تبادل الهالوجين، والذي يتضمن تفاعل كلوريد التنتالوم (V) مع يوديد الألومنيوم (III) الزائد عند 400 درجة مئوية لإعطاء التنتالوم (الخامس) يوديد

يمكن إنتاج اليودات المنخفضة إما من خلال التحلل الحراري أو عدم التناسب، أو عن طريق تقليل اليوديد الأعلى بهيدروجين أو معدن، على سبيل المثال:
![{\displaystyle {\ce {TaI5{}+Ta->[{\text{thermal gradient}}][{\ce {630^{\circ }C\ ->\ 575^{\circ }C}}]Ta6I14}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2bccb303062c4ab95661541d583e04d60a434c25)
معظم اليودات الموجودة في معادن ما قبل الانتقال (المجموعات 1و2 و 3، جنبًا إلى جنب مع اللانثانيدات والأكتينيدات في حالات الأكسدة 2+ و3+) هي في الغالب أيونية، بينما تميل اللافلزات إلى تكوين اليودات الجزيئية التساهمية، كما تفعل المعادن في حالات الأكسدة العالية من +3 وما فوق. تميل اليويدات الأيونية MI n إلى الحصول على أدنى نقاط انصهار وغليان بين هاليدات MX n لنفس العنصر، لأن قوى الجذب الكهروستاتيكية بين الكاتيونات والأنيونات تكون أضعف بالنسبة لأنيون اليوديد الكبير. في المقابل، تميل اليودات التساهمية إلى الحصول على أعلى نقاط انصهار وغليان بين هاليدات العنصر نفسه، نظرًا لأن اليود هو أكثر الهالوجينات قابلية للاستقطاب ، ولأنه يحتوي على معظم الإلكترونات من بينها ، يمكن أن يساهم بشكل أكبر في قوى فان دير فال. بطبيعة الحال ، تكثر الاستثناءات في اليود الوسيط حيث يفسح اتجاه واحد الطريق للآخر. وبالمثل ، فإن قابلية الذوبان في الماء لليويدات التي يغلب عليها الأيونات (مثل البوتاسيوم والكالسيوم) هي الأكبر بين الهاليدات الأيونية لهذا العنصر، بينما تكون ذوبان اليودات التساهمية (مثل الفضة) هي الأدنى من ذلك العنصر. على وجه الخصوص، يوديد الفضة غير قابل للذوبان في الماء وغالبًا ما يستخدم تكوينه كاختبار نوعي لليود.
هاليدات اليود
يشكل اليود جميع المواد البينية ثنائية الذرة الممكنة، وهي ثلاثي فلوريد وثلاثي كلوريد، بالإضافة إلى خماسي فلوريد، وبشكل استثنائي بين الهالوجينات، سباعي فلوريد. يتم أيضًا تمييز العديد من المشتقات الكاتيونية والأنيونية، مثل مركبات النبيذ الأحمر أو البرتقالية الزاهية لـ ICl2+ والمركبات ذات اللون البني الداكن أو الأسود المسترجن من I2Cl+ . وبصرف النظر عن هذه، بعض هالوجين زائف ومن المعروف أيضا، مثل السيانوجين يوديد (ICN) واليود ثيوسيانات (ISCN)، واليود أزيد (IN 3).
أحادي فلوريد اليود (IF) غير مستقر في درجة حرارة الغرفة ولا يتناسب بسهولة وبلا رجعة مع اليود وخماسي فلوريد اليود، وبالتالي لا يمكن الحصول عليه نقيًا. يمكن تصنيعه من تفاعل اليود مع غاز الفلورين في ثلاثي كلورو فلورو ميثان عند 45- درجة مئوية، مع ثلاثي فلوريد اليود في ثلاثي كلورو فلورو ميثان عند 78- درجة مئوية، أو مع فلوريد الفضة (I) عند 0 درجة مئوية.من ناحية أخرى، فإن أحادي كلوريد اليود (ICl) واليود أحادي البروميد (IBr) مستقران بشكل معتدل. تم اكتشاف المركب الأول، وهو مركب أحمر-بني متطاير ، بشكل مستقل من قبل جوزيف لويس جاي-لوساك وهامفري ديفي في 1813-1814 بعد وقت قصير من اكتشاف الكلور واليود ، وهو يحاكي بروم الهالوجين الوسيط جيدًا لدرجة أن يوستوس فون ليبيغ كان مضللاً في الخلط بين البروم (الذي وجده) أحادي كلوريد اليود. يمكن تحضير أحادي كلوريد اليود وأحادي بروميد اليود ببساطة عن طريق تفاعل اليود مع الكلور أو البروم عند درجة حرارة الغرفة وتنقيته بواسطة التبلور الجزئي. كلاهما متفاعل للغاية ويهاجم حتى البلاتين والذهب، ولكن ليس البورون والكربون والكادميوم والرصاص والزركونيوم والنيوبيوم والموليبدينوم والتنغستن. تفاعلهم مع المركبات العضوية يعتمد على الظروف. يميل بخار كلوريد اليود إلى كلورة الفينول وحمض الساليسيليك، لأنه عندما يخضع كلوريد اليود للتفكك المتجانس، ينتج الكلور واليود ويكون الأول أكثر تفاعلًا. ومع ذلك، ينتج عن كلوريد اليود في محلول رباعي كلورو الميثان أن المعالجة باليود هي التفاعل الرئيسي، حيث يحدث الآن الانشطار غير المتجانس لرابطة I-Cl ويهاجم I+ الفينول ككهربائي. ومع ذلك، يميل أحادي بروميد اليود إلى بروم الفينول حتى في محلول رباعي كلورو الميثان لأنه يميل إلى التفكك في عناصره في المحلول، والبروم أكثر تفاعلاً من اليود. عندما يتفكك السائل، أحادي كلوريد اليود واليود أحادي البروميد إلى أنيون (X = Cl ، Br)؛ وبالتالي فهي موصلات مهمة للكهرباء ويمكن استخدامها كمذيبات مؤينة.
أكاسيد اليود و oxoacids
التطبيقات
يذهب حوالي نصف اليود المنتج إلى مركبات اليود العضوية المختلفة، ويبقى 15٪ أخرى كعنصر نقي، ويستخدم 15٪ أخرى لتكوين يوديد البوتاسيوم، و15٪ أخرى لمركبات اليود غير العضوية الأخرى. من بين الاستخدامات الرئيسية لمركبات اليود المحفزات ومكملات الأعلاف الحيوانية والمثبتات والأصباغ والملونات والأصباغ والأدوية والصرف الصحي (من صبغة اليود) والتصوير الفوتوغرافي؛ تشمل الاستخدامات البسيطة منع الضباب الدخاني، واستمطار السحب، واستخدامات مختلفة في الكيمياء التحليلية.
تحليل كيميائي
غالبًا ما يتم استخدام أنيونات اليود واليود للتحليل الحجمي الكمي، على سبيل المثال في قياس اليود. وكثيرا ما يستخدم اليود والنشا شكل الأزرق معقدة، وهذا رد فعل على اختبار إما النشا أو اليود، وبوصفها مؤشرا في قياس يودي. لا يزال اختبار اليود للنشا مستخدمًا للكشف عن الأوراق النقدية المزيفة المطبوعة على ورق يحتوي على النشا.
قيمة اليود هي كتلة اليود بالجرام التي تستهلكها 100 جرام من مادة كيميائية عادة دهون أو زيوت. غالبًا ما تستخدم أرقام اليود لتحديد مقدار عدم التشبع في الأحماض الدهنية. يحدث عدم التشبع هذا في شكل روابط مزدوجة تتفاعل مع مركبات اليود. في علم الأحياء، حمض اللينوليك (C18: 2 n-6)، أوميغا 6 وألفا لينولينيك (C18: 3 n-3) أوميغا 3، حمض الأراكيدونيك (AA) - أوميغا 6 (C20: 4n-6)، وحمض الدوكوساهيكسانويك (DHA) - أوميغا 3 (C22: 6n-3) المركب مع اليودوليبيدات اليود التي تم تطويرها بين أغشية الخلايا أثناء تطور الحياة، وهي مهمة في آلية موت الخلايا المبرمج والتسرطن والأمراض التنكسية.
رباعي كلوريد البوتاسيوم (II)، K 2 HgI 4، يُعرف أيضًا باسم كاشف نيسلر. غالبًا ما يستخدم كاختبار بقعة حساسة للأمونيا. وبالمثل، يتم استخدام Cu 2 HgI 4 ككاشف ترسيب لاختبار قلويدات. يستخدم محلول اليود القلوي المائي في اختبار اليود لكيتونات الميثيل.
التحليل الطيفي
يتكون أطياف جزيء اليود، I 2، من عشرات الآلاف من الخطوط الطيفية الحادة في مدى الطول الموجي 500-700 نانومتر. لذلك فهو مرجع طول موجي شائع الاستخدام (معيار ثانوي). من خلال القياس بتقنية خالية من الدوبلر الطيفي مع التركيز على أحد هذه الخطوط ، يكشف التركيب فائق الدقة لجزيء اليود عن نفسه. تم حل الخط الآن بحيث يمكن قياس 15 مكونًا (من الأرقام الكمية الدورانية الزوجية، J حتى)، أو 21 مكونًا (من الأرقام الكمومية الدورانية الفردية، J الفردية).
يستخدم يوديد السيزيوم ويوديد الصوديوم المشبع بالثاليوم في أجهزة التلألؤ البلورية للكشف عن أشعة جاما. الكفاءة عالية والتحليل الطيفي المشتت للطاقة ممكن، لكن الدقة ضعيفة نوعًا ما.
دفع المركبة الفضائية
في أوائل عام 2021، أجرت مجموعة فرنسية عرضًا توضيحيًا في المدار لمحرك أيوني يعمل بالطاقة الكهربائية للمركبة الفضائية، حيث تم استخدام اليود بدلاً من الزينون كمصدر للبلازما، من أجل توليد الدفع عن طريق تسريع الأيونات مع مجال إلكتروستاتيكي. يمكن بناء أنظمة الدفع التي تستخدم اليود كوقود دافع بشكل أكثر إحكاما، وبكتلة أقل (وتكلفة)، وتعمل بكفاءة أكبر من محركات الدفع الأيونية الشبكية التي تم استخدامها لدفع المركبات الفضائية السابقة، مثل مجسات هايابوسا اليابانية، أو القمر الصناعي GOCE التابع لوكالة الفضاء الأوروبية، أو مهمة DART التابعة لناسا، والتي استخدمت جميعها الزينون ككتلة تفاعل. يجب أن يسمح استخدام اليود بدلاً من ذلك بتطبيق أكثر انتشارًا لتكنولوجيا الدفع الأيوني، لا سيما مع المركبات الفضائية الأصغر حجمًا.
وفقًا لوكالة الفضاء الأوروبية، «يمكن أن يساعد هذا الابتكار الصغير، ولكن المُدمِّر، في تطهير السماء من النفايات الفضائية، من خلال تمكين الأقمار الصناعية الصغيرة من التدمير الذاتي بثمن بخس وبسهولة في نهاية مهامها، من خلال توجيه نفسها إلى الغلاف الجوي حيث سوف تحترق».
الطب
عنصر اليود
يستخدم اليود العنصري كمطهر إما كعنصر، أو كأنيون ثلاثي اليود قابل للذوبان في الماء I 3- إنشاؤه في الموقع عن طريق إضافة اليود إلى اليود غير القابل للذوبان في الماء بشكل سيئ (التفاعل الكيميائي العكسي يجعل بعض اليود الحر متاحًا لتعقيم). يمكن أيضًا استخدام عنصر اليود لعلاج نقص اليود.
في المقابل، يمكن إنتاج اليود من اليود، الذي يحتوي على اليود المركب مع عامل مذاب (يمكن اعتبار أيون اليود بشكل غير محكم مثل اليود في محاليل الماء ثلاثي اليود). من أمثلة هذه المستحضرات ما يلي:
- صبغة اليود: اليود في الايثانول أو اليود ويوديد الصوديوم في خليط من الايثانول والماء.
- اليود المائي: اليود واليوديد في الماء وحده، مكونًا في الغالب ثلاثي اليود. على عكس صبغة اليود، يحتوي اليود المائي على كمية قليلة من مكون اليود الحر (I 2).
- بوفيدون اليود (يودوفور).
إن المفعول المضاد للميكروبات لليود سريع ويعمل بتركيزات منخفضة، وبالتالي يستخدم في غرف العمليات. طريقة عملها المحددة غير معروفة. يخترق الكائنات الحية الدقيقة ويهاجم أحماض أمينية معينة (مثل السيستين والميثيونين) والنيوكليوتيدات والأحماض الدهنية، مما يؤدي في النهاية إلى موت الخلايا. كما أن لديها المضادة للفيروسات العمل، ولكن الفيروسات وفيروسات صغيرة أقل حساسية من الدهون يلفها الفيروسات. اليود ربما هجمات سطح البروتينات من يلفها الفيروسات، وأنه يجوز أيضا زعزعة غشاء الأحماض الدهنية عن طريق تفاعل مع غير المشبعة سندات الكربون.
تركيبات أخرى
في الطب، يتم استخدام محلول مشبع من يوديد البوتاسيوم لعلاج الانسمام الدرقي الحاد. يستخدم أيضًا لمنع امتصاص اليود 131 في الغدة الدرقية، عندما يتم استخدام هذا النظير كجزء من الأدوية المشعة (مثل iobenguane) التي لا تستهدف الغدة الدرقية أو أنسجة الغدة الدرقية.
اليود 131 (عادة في صورة يوديد) هو أحد مكونات السقوط النووي، وهو خطير بشكل خاص بسبب ميل الغدة الدرقية لتركيز اليود المبتلع والاحتفاظ به لفترات أطول من نصف العمر الإشعاعي لهذا النظير وهو ثمانية أيام. لهذا السبب، قد يُطلب من الأشخاص المعرضين لخطر التعرض لليود المشع البيئي (اليود 131) في السقوط أن يأخذوا أقراص يوديد البوتاسيوم غير المشعة. الجرعة النموذجية للبالغين هي 130 ملغ مضغوطة لكل 24 ساعة تؤمن 100 ملغ ملغ (100000 ميكروغرام) من اليود الأيوني. (الجرعة اليومية المعتادة من اليود للصحة العادية هي 100 ميكروغرام ، انظر «المدخول الغذائي» أدناه.) إن ابتلاع هذه الجرعة الكبيرة من اليود غير المشع يقلل من امتصاص الغدة الدرقية لليود المشع.

الدور البيلوجي
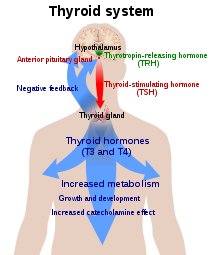
اليود عنصر أساسي للحياة ، وبالعدد الذري Z = 53، هو أثقل عنصر تحتاجه الكائنات الحية بشكل شائع. (اللنثانوم وغيرها من اللانثانيدات، فضلا عن التنغستن مع Z = 74، وتستخدم من قبل عدد قليل من الكائنات الحية الدقيقة.) وهو مطلوب لتخليق هرمونات الغدة الدرقية المنظمة للنمو ، الثيروكسين وثلاثي يودوثيرونين (T 4 و T 3 على التوالي ، سميت باسم عدد ذرات اليود). يؤدي نقص اليود إلى انخفاض إنتاج T 3 و T 4 وما يصاحب ذلك من تضخم في أنسجة الغدة الدرقية في محاولة للحصول على المزيد من اليود ، مما يسبب المرض المعروف باسم تضخم الغدة الدرقية البسيط. الشكل الرئيسي لهرمون الغدة الدرقية في الدم هو هرمون الغدة الدرقية (T 4)، والذي يمتاز بنصف عمر أطول من T 3 . في البشر ، تتراوح نسبة T 4 إلى T 3 في الدم بين 14: 1 و 20: 1. T 4 يتم تحويلها إلى T نشط 3 (3-4 مرات أكثر قوة مما T 4) داخل الخلايا بواسطة دييودوناز (5'-iodinase). تتم معالجتها أيضًا عن طريق نزع الكربوكسيل وإزالة اليود لإنتاج يودوثيرونامين (T 1 أ) وثيرونامين (T 0 أ '). جميع الأشكال الإسوية الثلاثة للديودينازات هي عبارة عن إنزيمات تحتوي على السيلينيوم ؛ وبالتالي السيلينيوم الغذائية أمر ضروري لT 3 الإنتاج.
يمثل اليود 65٪ من الوزن الجزيئي لـ T 4 و 59٪ من T 3. من خمسة عشر إلى 20 ملغم من اليود يتركز في أنسجة الغدة الدرقية والهرمونات، ولكن يوجد 70٪ من اليود في الجسم في الأنسجة الأخرى ، بما في ذلك الغدد الثديية والعينين والغشاء المخاطي في المعدة والغدة الصعترية الجنينية والسائل المخي الشوكي والضفيرة المشيمية وجدران الشرايين عنق الرحم والغدد اللعابية. في خلايا تلك الأنسجة ، يدخل اليود مباشرة عن طريق متناظر يوديد الصوديوم (NIS). يرتبط عمل اليود في أنسجة الثدي بنمو الجنين وحديثي الولادة ، ولكنه (على الأقل) غير معروف جزئيًا في الأنسجة الأخرى.
التوصيات الغذائية
إن كمية اليود الموصى باستهلاكها من قبل الأكاديمية الوطنية للطب تتراوح بين 100 و130 ميكروغرام يومياً للرضّع حتى سن 12 شهر، 90 ميكروغرام للأطفال حتى عمر الثماني سنوات، 130 ميكروغرام للأطفال حتى عمر 13 سنة، 150 ميكروغرام للبالغين، 220 ميكروغرام للحوامل، 290 ميكروغرام للمرضّعات. إن المستوى الأعلى المسموح للبالغين هو 1100 ميكروغرام.
فوائد اليود
اليود هو أحد العناصر الغذائية الهامة اللازمة لعملية التمثيل الغذائي وله أثار هامة علي الغدة الدرقية التي تكافح الجراثيم الضارة. يتم تخزين حوالي % 65 من اليود في جسم الإنسان في الغدة الدرقية. وله العديد من الفوائد الصحية التي تلعب دوراً هاماً في أداء عمل الغدة الدرقية، التي تفرز الهرمونات وتتحكم في معدل الأيض الأساسي للجسم. وفي الحقيقة الغدة الدرقية بدون اليود لا تفرز الهرمونات كما أن اليود يتواجد في الخضروات خصوصا الطماطم والأسماك بتركيز عالي جدا. نقص اليود يسبب تضخم الغدة الدرقية اليود مهم جدا ملح اليود ينصح بتناوله الأطباء .
انظر أيضًا
- يوديد
- بوفيدون يودي (مطهر من اليود)
- يودوفورم (مركب من اليود)
- ملح معالج باليود
المراجع
| H | He | |||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| معرفات كيميائية |
|
|---|